【7.8.1.7】CTLA-4(CD152)
CTLA-4(cytotoxic T-lymphocyte-associated protein 4,细胞毒性 T 淋巴 细胞相关蛋白 4)
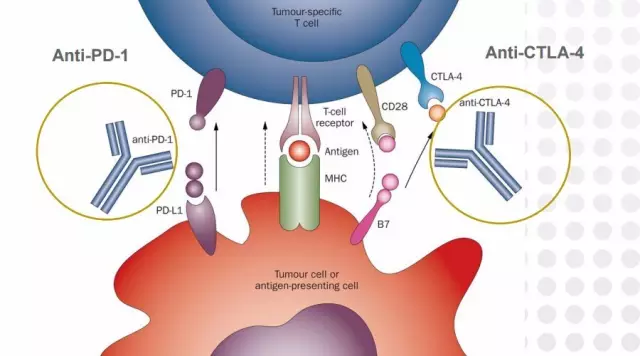
细胞毒T淋巴细胞抗原4(CTLA-4)又名CD152,是由CTLA-4基因编码的一种跨膜蛋白质,表达于活化的CD4+和CD8+T细胞。CTLA-4与其配体B7分子结合后产生抑制性信号,抑制T细胞激活,使肿瘤细胞免受T淋巴细胞攻击。因此阻断CTLA-4的免疫效应可刺激免疫细胞大量增殖,从而诱导或增强抗肿瘤免疫反应。目前将CTLA-4抗体和PD-1抗体联合治疗已经成为抗肿瘤治疗的热点。
一、CTLA-4的结构及功能
CTLA-4基因定位于人体2号染色体上,主要表达于活化的调节性T细胞(Treg)表面,与T细胞表面的协同刺激分子受体(CD28)具有高度的同源性。CTLA-4和CD28均为免疫球蛋白超家族成员,二者与相同的配体CD86(B7-2)和CD80(B7-1)结合。CD28表达于T细胞,为T细胞的激活提供协同刺激信号,促进T细胞的活化;与CD28的功能相反,CTLA-4与B7分子结合后抑制T细胞活化。
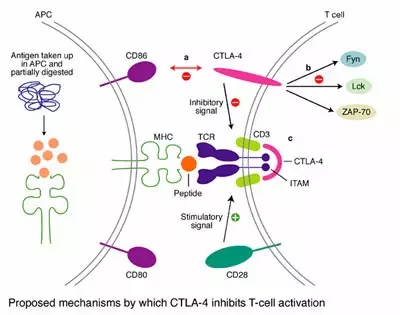
二、CTLA-4的作用机制
CTLA-4的作用机制尚未完全阐明,主要有以下几种可能:
- 通过其胞外域起竞争配体作用:CTLA4与B7分子具有高度的亲合力,与CD28竞争结合抗原提呈细胞(APC)上的B7家族分子,阻断CD28与B7的信号传导通路,防止CD28分子促进T细胞激活。
- 抑制IL-2的产生,实现负性调节作用。
- 抑制细胞周期:CTLA-4能够抑制T细胞从G期进入S期,从而抑制T细胞的增殖、活化。
- 干扰信号转导:CTLA-4通过与蛋白磷酸酶-2(PP2A)及蛋白酪氨酸磷酸酶(SHP2)相互作用干扰TCR信号,同时CTLA-4与PI3K结合,导致Akt磷酸化,引起促凋亡因子BAD失活,并上调抗凋亡因子Bcl-xL和Bcl-2,在免疫耐受中扮演关键性的角色。
三、CTLA-4的应用
鉴于CTLA-4的特点,临床上有正反两个方向的应用:
- CTLA-4模拟抗体可抑制免疫,治疗自身免疫性疾病
- CTLA-4拮抗型抗体可激活免疫细胞治疗肿瘤。
3.1 治疗自身免疫性疾病
自身免疫是指机体免疫系统对自身成分发生免疫应答,产生自身抗体或自身反应性T淋巴细胞。若自身耐受机制遭破坏,自身免疫应答的质和量发生异常,则自身抗体和自身反应性淋巴细胞可攻击并破坏自身组织细胞,机体出现病理改变和相应临床表现,此即自身免疫性疾病。CTLA-4模拟抗体能够抑制免疫,治疗自身免疫性疾病。CTLA-4模拟抗体Abatacept已用于治疗类风湿性关节炎。新一代的CTLA-4和IgG融合蛋白-Belatacept是FDA批准的抑制肾移植后排斥的首选药物。
3.2 治疗肿瘤
CTLA-4抗体产生的抗肿瘤作用包括两种机制:①干扰肿瘤特异性效应细胞如CD8细胞,导致其克隆扩增。②去除肿瘤诱导的调节性T细胞(Treg),Treg细胞可抑制肿瘤相关抗原的免疫反应。
CTLA-4拮抗型抗体可以阻断内源性CTLA-4对免疫细胞的抑制作用,保留B-7受体和CD28结合从而激活免疫细胞提升免疫监视能力,用于肿瘤免疫治疗。多临床前期的试验证明,CTLA-4抗体对多种自身免疫性疾病,多种肿瘤包括:肺癌、胃癌、肠道肿瘤、胰腺癌、前列腺癌、卵巢肿瘤等等。
目前两种靶向CTLA-4的抗体Ipilimumab和Tremelimumab均已进入Ⅲ期临床试验,已广泛用于治疗黑色素瘤、肾癌、前列腺癌、肺癌等。Ipilimumab(Yervoy)是靶向作用于CTLA-4的全人源化单克隆抗体,通过作用于APC与T细胞的活化途径而间接活化抗肿瘤免疫反应,达到清除癌细胞的目的。Tremelimumab又称为CP657206,是一种人源化CTLA-4的抗体,它是一种人免疫球蛋白G2抗体。Ⅰ/Ⅱ期临床研究结果显示两种抗体无论是抗体单药还是联合IL-2,gp100疫苗或化疗均显示安全有效。
1. 靶点机制(图 37)
通过抑制免疫检查点活性,释放肿瘤微环境中的免疫“刹车”,激活抗肿瘤免疫反应是 近几年肿瘤免疫治疗的热点。目前,研究较成熟的免疫检查点是 PD-1/PD-L1 和 CTLA-4。 在正常的免疫反应过程中,T 细胞活化需要 2 个信号:
1.抗原呈递细胞(antigen presenting cell,APC)通过抗原-MHC 分子复合物特异性识别、结合 T 细胞表面的 TCR-CD3 分子, 向 T 细胞传递活化的第一信号, 2. APC 表面的 B7 与静止 T 细胞表面的协同刺激分子受体 CD28 结合,为 T 细胞活化提供第二信号。
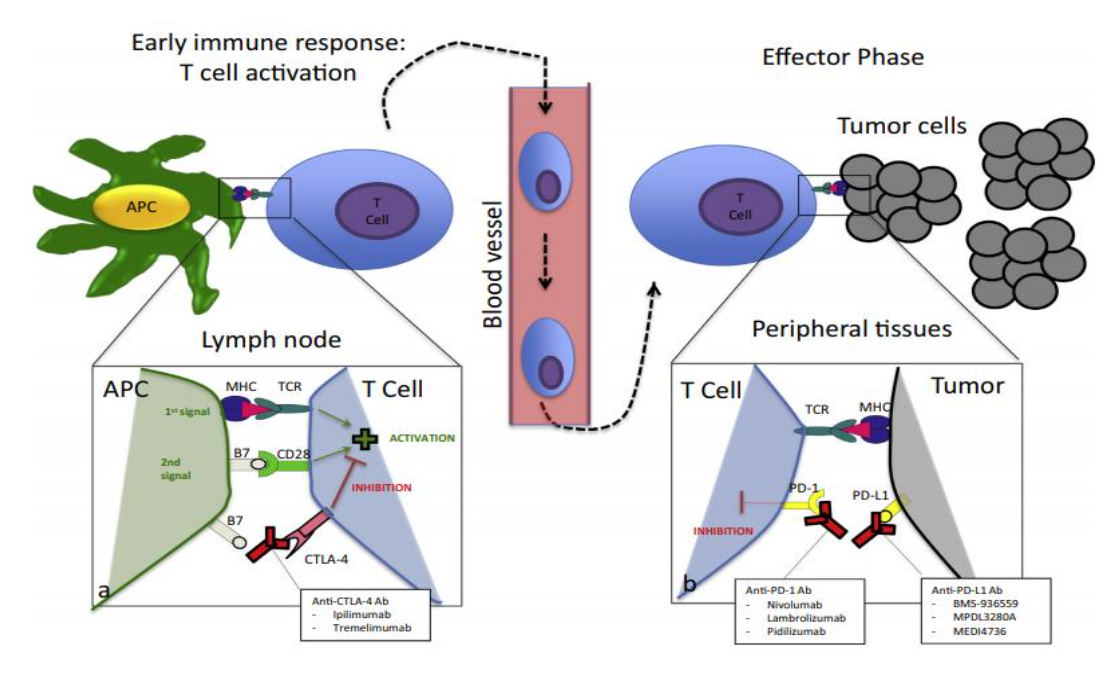
资料来源:Chrisann Kyi,Michael A Postow.Checkpoint blocking antibodies in cancer immune-therapy[J]. FEBS Lett,2014,588(2):368-376.doi:10.1016/j.febslet.2013.10.015. Epub 2013 Oct23. PMID:24161671.
CTLA-4与协同刺激分子受体CD28高度同源,二者均可与APC表面配体CD86(B7- 2)/CD80(B7-1)结合,且 CTLA-4 对 B7 的亲和力明显高于 CD28。但与 CD28 不同, CTLA-4 与 APC 表面配体结合后向 T 细胞传导抑制信号,阻断 CD28 对 T 细胞的协同刺 激作用,抑制 T 细胞活化。此外,CTLA-4 还可抑制 CD25 的表达发挥免疫抑制作用。因 此,应用抗 CTLA-4 单抗可解除 CTLA-4 对 T 细胞的抑制作用,上调 T 细胞的活化增殖, 诱导细胞毒性 T 淋巴细胞恢复其杀伤肿瘤细胞的功能。全球首个获批的抗 CTLA-4 单抗 是百时美施贵宝的伊匹木单抗,于 2011 年由美国 FDA 批准上市。目前,全球共有 32 款 涉及 CTLA-4 靶点的在研药物,其中阿斯利康的替西利姆单抗(Tremelimumab)是市场认 为最有可能上市的第二款 CTLA-4 产品。目前国内唯一上市的 CTLA-4 是于 2021 年 6 月 获批的伊匹木单抗。
2. 临床研究申报概况
在 2022 年度申报的临床研究中,有 20 余项研究涵盖抗 CTLA-4 治疗,其中国际多中 心临床研究 3 项。共涉及 8 款 CTLA-4 抗体类药物,其中 5 款为 CTLA-4 单克隆抗体,分 别为阿斯利康的 Tremelimumab、天演药业的 ADG126 注射液、宜明昂科的 IMM27M 注 射液、恒瑞医药的 SHR-8068 注射液、百奥赛图的 YH001 注射液。除 Tremelimumab 有 2 项研究为III期临床设计(EMERALD-3 研究、度伐利尤单抗联合 Tremelimumab 一线治疗 不可切除肝细胞癌)外,其余 CTLA-4 单抗药物尚处于早期临床研究阶段。此部分II期及 III期临床研究设计均为双免联合治疗。
双抗类药物分别为康方生物的 AK104 注射液、齐鲁制药的 QL1706 注射液、康宁杰 瑞的 KN046 注射液,前者为 CTLA-4/PD-1 双抗,QL1706 为双免疫的组合抗体,KN046 为 CTLA-4/PD-L1 双抗。AK104 基于宫颈癌含铂化疗后二线治疗的适应证上市,目前有 3 项研究进入III期临床,分别为 AK104 联合化疗用于晚期胃癌一线治疗、AK104 用于高复 发风险肝细胞癌根治术后辅助治疗、AK104 联合同步放化疗治疗局部晚期宫颈癌。QL1706 也有 2 项研究进入III期临床,分别为 QL1706 联合含铂化疗辅助治疗完全手术切除后的 II~IIIb 期非小细胞肺癌、QL1706 联合紫杉醇-顺铂/卡铂加或不加贝伐珠单抗用于一线 治疗持续、复发或转移性宫颈癌。其余的I期及II期研究设计以双抗药物联合化疗或其他 小分子靶向药为主。
本年度 CTLA-4 抗体类药物开发的适应证主要集中在实体瘤、小细胞肺癌、非小细胞 肺癌、宫颈癌、肝细胞癌、肾细胞癌、鼻咽癌、结直肠癌,包含新辅助治疗、辅助治疗、 一线治疗、二线治疗及后线治疗。
3. 简评
全球 CTLA-4 药物百家争鸣,开发的适应证繁杂多样。但因 CTLA-4 单抗单药治疗应 答率有限,2022 年度临床研究布局依然以联合治疗为主,其中以与 PD-1/PD-L1 抑制剂联合更为常见,并且双抗类药物的临床研究也在进一步做加法(与化疗或小分子靶向药进行 联合)。多种治疗手段的联合势必会进一步增加不良反应的发生率。未来需进一步探索如 何让 CTLA-4 抑制剂的联合治疗增效但不加毒,才能最终推进其在临床中的广泛应用。
参考资料
- https://mp.weixin.qq.com/s/Fpz2To1FwfOt8fdJf1xQ-A
- 《2022年度中国抗肿瘤新药临床研究评述》
