【1.3.3.1】免疫细胞--B淋巴细胞
B 淋巴细胞是由人和哺乳动物骨髓或禽类法氏囊中始祖 B 细胞分化成熟而 来,故称骨髓/囊依赖性淋巴细胞(bone marrow/bursa of fabricius dependent lymphocyte),简称 B 淋巴细胞或 B 细胞。根据分布、表面标志和功能特征,可 将 B 细胞分为以下两个亚群:
- B1 细胞是执行非特异免疫应答的固有免疫细胞;
- B2 细胞是执行特异性体液免疫应答的 B 细胞,也是启动适应性体液免疫应答的 专职抗原提呈细胞。
一、B 细胞在骨髓中的发育成熟
人和哺乳动物的 B 细胞在骨髓中以抗原非依赖的方式发育成熟,经历了始祖 B 细胞、前 B 细胞、未成熟 B 细胞和成熟 B 细胞四个阶段,在上述 B 细胞四个发 育阶段 CD19 和 CD45R 表达贯穿始终。

1.1 始祖 B 细胞阶段
始祖 B 细胞(pro-B cell)由骨髓淋巴干细胞衍生而 来,其表面具有多种黏附分子、干细胞生长因子受体(SCF-R)和白细胞介素-7 受体(IL-7R);而不表达 B 细胞抗原受体(BCR/mIgM)。骨髓微环境中始祖 B 细 胞通过表面迟现抗原-4(very late antigen-4,VLA-4)等黏附分子与骨髓基质 细胞表面 VCAM-1 等相应黏附分子结合相互作用,进而通过表面 SCF-R 和 IL-7R 接受骨髓基质细胞表面膜型 SCF(mSCF)及其分泌的 IL-7 刺激后,分化发育为 前 B 细胞。
1.2 前 B 细胞阶段
前 B 细胞(pre-B cell)胞质中出现 IgM 的重链分子即 μ链,膜表面出现少量由μ链与替代性轻链组成的前 B 细胞受体。此种前 B 细胞 受体没有抗原识别结合能力,而与前 B 细胞的进一步分化发育有关。
1.3 未成熟 B 细胞阶段
未成熟 B 细胞由前 B 细胞分化而来,在其胞质中出 现完整的 IgM 单体分子,同时细胞表面出现功能性 B 细胞受体,即由膜表面单体 IgM(BCR/mIgM)与 Igα/Igβ 异二聚体非共价结合组成的 BCR-Igα/Igβ 复合 体。当未成熟 B 细胞通过表面 BCR-Igα/Igβ 复合体与骨髓基质细胞表面自身抗 原高亲和力结合相互作用后,可使其停止发育、不再对相应抗原产生应答,即使 体内未成熟自身反应性 B 细胞形成中枢免疫耐受。但某些与骨髓基质细胞表面自 身抗原低亲和力结合的未成熟 B 细胞能够继续分化发育,作为具有免疫潜能的自 身反应性 B 细胞存在于体内。
1.4 成熟 B 细胞阶段
成熟 B 细胞主要由那些未与自身抗原结合的未成熟 B 分化发育而成。此种 B 细胞膜表面同时表达两种 B 细胞受体,即由 mIgM 和 mIgD 分别与 Igα/Igβ 异二聚体非共价结合组成的 BCR-Igα/Igβ 复合体和其他膜 分子。成熟 B 细胞即通常所说得 B 细胞是具有免疫功能的淋巴细胞,他们接受相 应抗原刺激后可产生特异性体液免疫应答。初始 B 细胞(naive B cell)是指离 开骨髓进入外周后,从未与其特异性抗原相遇,即对相应抗原尚未产生应答的成 熟 B 细胞。
二、B 淋巴细胞表面标志及其主要作用
2.1 B 细胞作为免疫应答细胞,与其识别抗原和活化相关的分子
2.1.1 B 细胞受体(B cell receptor,BCR)
是 B 细胞表面特异性识别抗原 的受体,也是所有 B 细胞的特征性表面标志,其化学本质是膜表面免疫球蛋白 (mIg)。B1 细胞仅表达 mIgM;B2 细胞即本节介绍的 B 细胞同时表达 mIgM 和 mIgD。 如图 10-11 所示:BCR 是由二条相同的重链和两条相同的轻链通过链间二硫键共 价相连组成的一个四肽链分子:BCR 胞外区肽链 N 端为可变区,其内各有三个氨 基酸组成和排列顺序高度易变的超变区,从而造就了 BCR 的高度多样性和对相应 抗原表位识别结合的高度特异性;BCR 胞内区短小,没有传递细胞活化信号的功 能,其疏水性跨膜区含带正电荷的氨基酸残基,借此能与跨膜区带负电荷氨基酸 残基的 Igα/Igβ 异二聚体非共价结合组成 BCR-Igα/Igβ 复合体。Igα/Igβ 异二聚体是由 CD79a 和 CD79b 两条肽链通过链间二硫键连接组成的跨膜蛋白,其 胞内区含 ITAM 结构域,参与细胞活化信号的传递。
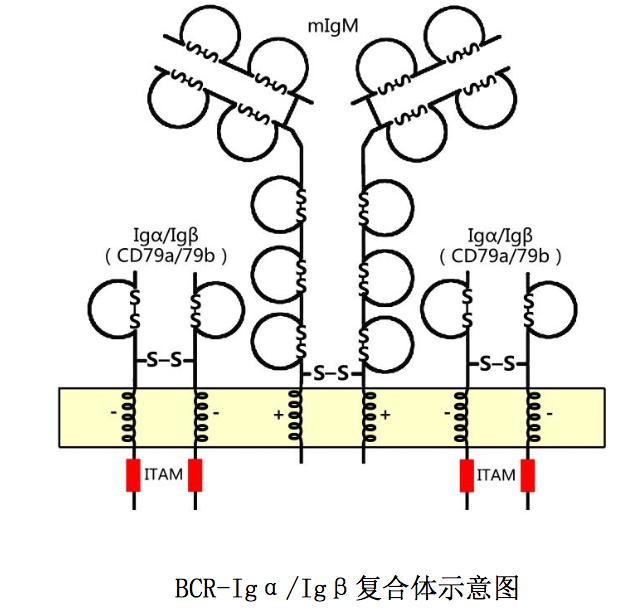
B 细胞表面 BCR-Igα/Igβ复合体与 T 细胞表面 TCR-CD3 复合体不同,可直 接识别结合暴露于抗原分子表面的 B 细胞表位。BCR-Igα/Igβ复合物介导的信 号转导如图 10-12 所示:B 细胞通过表面 BCR- Igα/Igβ复合体交联识别结合抗 原后,可使其胞浆内与 Igα/Igβ异二聚体尾肽相关的蛋白酪氨酸激酶(BLK、 Fyn 或 Lyn)活化,导致 Igα/Igβ胞质区 ITAM 磷酸化。磷酸化 ITAM 可趋化募集 Syk 激酶,使之与双重磷酸化 ITAM 结合后,通过自身磷酸化作用而被激活(图 10-12B),启动 B 细胞后续活化信号的转导。

2.1.2 BCR 辅助受体
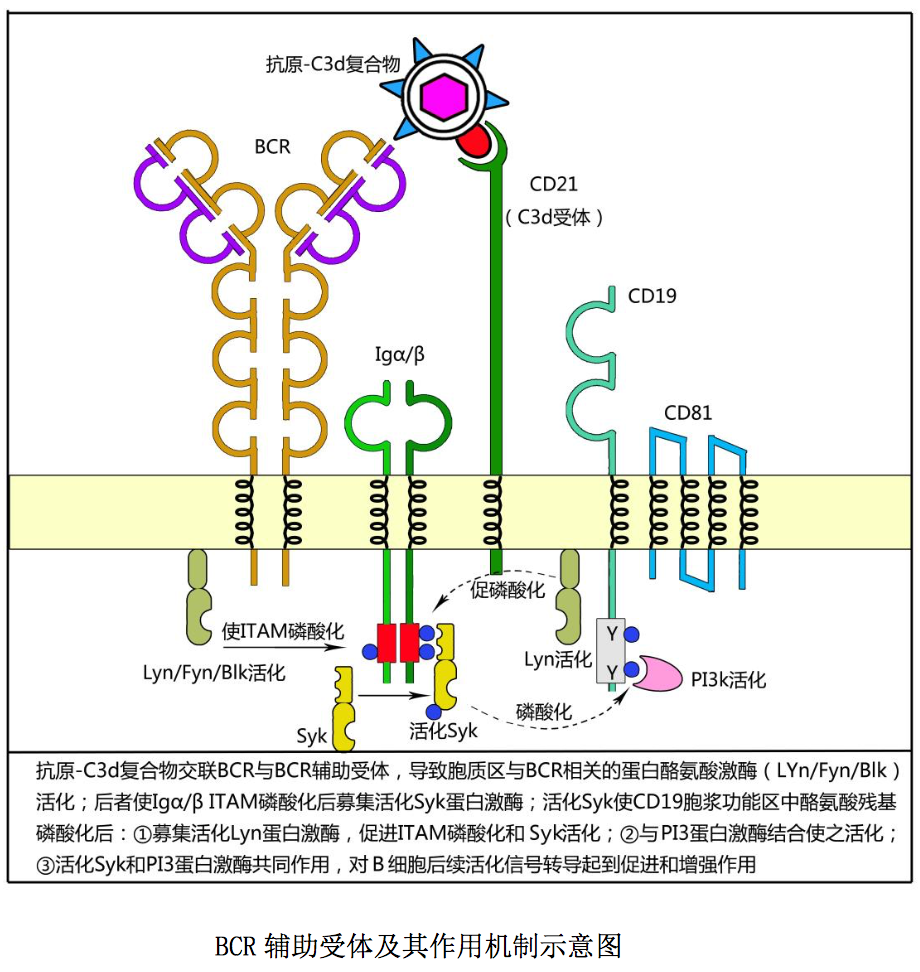
CD19-CD21-CD81 复合体是 B 细胞表面的 BCR 辅助受体 (图 10-13),其中 CD19 分子在 B 细胞谱系发育的各个阶段和活化 B 细胞表面 均可表达(浆细胞除外),是 B 细胞特有的表面标志;CD21 分子是补体 C3 裂解 产物 C3d 的受体;CD19 与 CD21 紧密相连,其胞质功能区含酪氨酸残基、参与 B 细胞活化信号的转导;CD81 为跨膜蛋白,其作用目前还不十分清楚,可能具有 稳定 D19-CD21-CD81 复合体的作用。
外周免疫器官淋巴滤泡中的 FDC 能够识别结合可溶性抗原与 IgG 抗体或 C3d 结合形成的免疫复合物或细菌裂解产物等可溶性抗原,并将上述免疫复合物或可 溶性抗原长期滞留于细胞表面,为 B 细胞识别结合抗原奠定了基础。BCR 及其辅 助受体作用如图 10-13 所示:1B 细胞通过表面 BCR-Igα/Igβ 复合体及其辅助 受体(CD21-CD19-CD81 复合体)与抗原-C3d 复合物中相应抗原表位和 C3d 交联 结合,可使其胞质区与 BCR 相关的蛋白酪氨酸激酶 BLK、Fyn 或 lyn 活化,并由 此导致 Igα/Igβ 胞质区 ITAM 磷酸化;2胞质区磷酸化 ITAM 可趋化募集并与 Syk 蛋白激酶结合使之活化(磷酸化);3活化 Syk 蛋白激酶可被 CD19 胞质功能区中的酪氨酸残基磷酸化,后者可进一步募集活 Lyu 蛋白激酶、促进 ITAM 磷酸 化和 Syk 激酶活化;同时能与 PI3 蛋白激酶结合使之活化;4活化 Syk 蛋白激酶 和 PI3 蛋白激酶共同作用,对 B 细胞后续活化信号转导起到促进和增强作用。研 究证实,在 BCR 辅助受体参与下,B 细胞对抗原刺激的敏感性可提高 1000 倍。
2.1.3 共刺激分子
B 细胞作为免疫应答细胞,其活化需要两种信号:1通过 表面 BCR-Igα/Igβ 复合体和 BCR 辅助受体识别结合抗原-C3d 复合物,诱导产 生的 B 细胞活化第一信号;2B 细胞通过表面 CD40 和 ICAM-1 等共刺激分子与 Th 细胞表面相应 CD40L 和 LFA-1 共刺激分子结合相互作用,诱导产生 B 细胞活化第 二信号。
(1)CD40 分子:是 B 细胞表面最重要的共刺激分子,属肿瘤坏死因子受体超 家族成员。B 细胞作为免疫应答细胞,在接受抗原刺激产生活化第一信号基础上, 通过表面 CD40 与活化 CD4+Th 细胞表面相应共刺激分子配体 CD40L 结合相互作 用,可诱导产生共刺激信号(B 细胞活化第二信号)使 B 细胞活化。
(2)ICAM-1 分子:是表达于 B 细胞表面的黏附分子,与活化 CD4+Th 细胞表 面相应黏附分子 LFA-1 结合可诱导产生共刺激信号,促进 B 细胞活化第二信号的 产生。
2.1.4 IgG Fc 受体II(FcγRII)
表达于 B 细胞、巨噬细胞和朗格汉斯细胞表 面,包括 FcγRII-A 和 FcγRII-B 两种类型。FcγRII-A 为活化性受体,B 细胞 通过表面FcγRII-A与抗原抗体复合物中IgG Fc段结合,不仅有助于B细胞对 抗原的捕获,而且能促进 B 细胞活化。FcγRII-B 是 B 细胞表面抑制性受体,其 胞质区含 ITIM 结构域,可转导 B 细胞活化抑制信号,下调体液免疫应答(详见 免疫调节)。
2.1.5 丝裂原受体
B 细胞表面具有脂多糖受体(LPS-R)、葡萄球菌 A 蛋白受 体(SPA-R)和美洲商陆受体(PWM-R);他们接受相应丝裂原刺激后可高表达 B7 等共刺激分子和其他粘附分子,并发生非特异性有丝分裂,即使多克隆 B 细胞转 化为淋巴母细胞。
2.1.6 细胞因子受体
静息 B 细胞接受抗原或丝裂原刺激后,可表达多种与其 活化、增殖、分化密切相关的 IL-1R,IL-4R,IL-5R,IL-6R,IL-10R 和 IFN-R 等 细胞因子受体;相关细胞因子与不同分化阶段 B 细胞表面相应细胞因子受体结合 后,可诱导 B 细胞活化、增殖,最终分化为合成分泌不同类型抗体的浆细胞。
2.2 B 细胞作为抗原提呈细胞,与其诱导 Th 细胞活化相关的分子
2.2.1 MHC 分子
B 细胞作为专职 APC,通过其表面 BCR 和 BCR 辅助受体将抗原 -C3d 复合物或其他可溶性抗原摄入胞内后,经外源性抗原加工途径,可将抗原 降解产物以抗原肽- MHCII类分子复合物的形式表达于细胞表面,供 CD4+Th 细胞 识别。当 CD4+Th 细胞通过表面 TCR-CD3 复合受体与 B 细胞表面抗原肽-MHCII类 分子复合物结合相互作用,可获得活化第一信号;通过表面 CD4 分子与 B 细胞表 面抗原肽 MHCII类分子复合物中 MHCII类分子β链β2 结构域结合,可增强 Th 细 胞与 B 细胞之间的相互作用,促进 T 细胞活化第一信号的产生。
2.2.2 共刺激分子
B7-1/B7-2 分子(CD80/CD86)和 ICAM-1 是表达于 B 细胞 表面的共刺激分子,其中 B7-1/B7-2 分子在诱导共刺激信号产生过程中起主导作 用。B 细胞作为专职 APC,在与 CD4+Th 细胞结合相互作用产生 T 细胞活化第一信 号基础上,通过 B7-1、2 和 ICAM-1 等共刺激分子与 CD4+Th 表面 CD28、LFA-1 等 相应配体分子结合相互作用,可诱导产生共刺激信号(T 细胞活化第二信号)导 致 B 细胞活化。
三、B 淋巴细胞亚群
根据 B 细胞发生、分布、表面标志和功能特征,可将其分为执行固有免疫应 答的 B1 细胞和执行适应性体液免疫应答的 B2 细胞,即通常所指的 B 细胞。
3.1 B1 细胞和 B2 细胞
1.B1细胞
在个体发育过程中出现相对较早,其产生与胚肝密切相关。 B1 细胞是具有自我更新能力的 CD5+、mIgM+ B 细胞,主要分布于腹膜腔、胸膜腔 和肠道固有层中。B1 细胞表面 BCR 较少多样性,主要识别细菌多糖类 TI 抗原和 某些变性自身抗原。B1 细胞产生抗体无需 Th 细胞协助;接受抗原刺激后 48 小 时即可产生相应低亲和力 IgM 类抗体。此类抗体可识别结合病原体表面共有多糖 抗原表位,对多种病原体产生非特异性免疫作用。
2.B2细胞
在个体发育过程中出现相对较晚,由骨髓多能造血干细胞分 化而成;B2 细胞没有自我更新能力,是执行适应性体液免疫应答的 CD5-、 mIgM+/IgD+ B 细胞,主要分布于外周免疫器官。B 细胞表面 BCR 具有高度多样性, 对可溶性蛋白质抗原的识别具有高度特异性;接受抗原刺激后需在 CD4+Th2 细胞 协助下才能产生相应抗体。B2 细胞介导的体液免疫应答与 B1 细胞相比有如下特 点:(1)抗体产生潜伏期较长;(2)产生以 IgG 类为主的高亲和力抗体;(3)产 生记忆 B 细胞,可引起再次免疫应答。B1 细胞和 B2 细胞发生、分布、表面标志 和功能特征比较见下表。

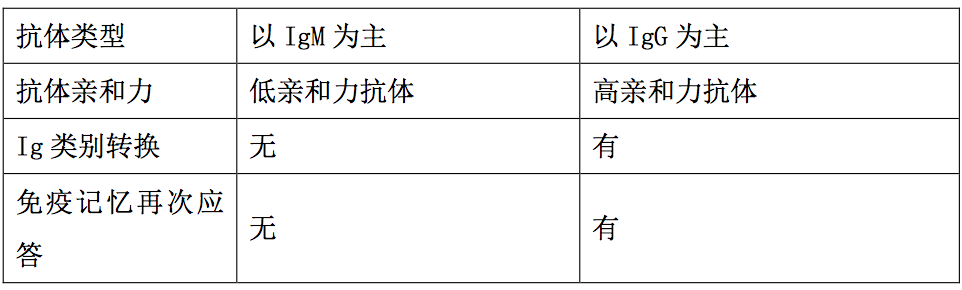
3.2 B2 细胞的主要生物学功能
3.2.1 摄取加工提呈抗原、启动适应性体液免疫应答
B2 细胞作为专职 APC, 可通过表面 BCR 直接识别结合进而摄取抗原,并将加工处理后形成的抗原性短肽 以抗原肽-MHCII类分子复合物形式转运到细胞表面,供抗原特异性 CD4+Th2 细胞 识别结合,从而启动适应性体液免疫应答。
3.2.2 合成分泌抗体、介导产生体液免疫效应
B2细胞作为免疫应答细胞, 接受相应抗原刺激后,在活化 CD4+Th 细胞协助下可增殖分化为浆细胞。浆细胞 是合成分泌抗体的效应细胞,在不同细胞因子作用下,可产生不同类型的抗体发 挥如下免疫效应:
- 与相应病原体或细菌外毒素特异性结合,可产生抑菌和中和 毒素作用;
- IgG 类抗体与相应病原体等抗原结合后,在吞噬细胞参与下可产生 促进吞噬的免疫调理作用;
- IgG 或 IgM 类抗体与抗原结合形成的免疫复合物激 活补体产生溶菌效应和 C3b 介导的调理作用;
- IgG 类抗体可与肿瘤或病毒感染 靶细胞表面相应抗原特异性结合后,可通过 ADCC 效应使上述靶细胞溶解破坏; 特异性 IgE 抗体通过其 Fc 段与肥大/嗜碱性粒细胞表面 FcεR 结合使之致敏后, 再次与相应变应原相遇可引发I型超敏反应。
参考资料
- 《医学免疫学》课件 新乡医学院 宋向凤、张国俊、徐春阳、孙爱平、孙书明、赵铁锁等老师
