【1.5】传感器细胞表达模式识别受体,提供自我和非我之间的初始区分
早在先天识别机制被发现之前,人们就认识到纯化的抗原(如蛋白质)在实验免疫中通常不会引起免疫反应;也就是说,它们不是免疫原性的。相反,对纯化蛋白的强烈免疫反应的诱导需要包含微生物成分,如杀死的细菌或细菌提取物,查尔斯·詹韦(Charles Janway)称之为免疫学家的“致命小秘密”(dirty little secret)(见附录I,第A-1节)。这种额外的材料被称为佐剂( adjuvant ),因为它有助于增强对免疫原的反应(佐剂在拉丁语中是“帮助”的意思)。我们现在知道,至少在部分情况下,需要佐剂来激活各种类型的传感器细胞上的固有受体,以帮助在没有感染的情况下激活T细胞
巨噬细胞、中性粒细胞和树突状细胞是检测感染并通过产生炎症介质启动免疫反应的重要传感器细胞,尽管其他细胞,甚至是适应性免疫系统的细胞,也可以发挥这一功能。如第1-3节所述,这些细胞表达有限数量的不变的固有识别受体,作为检测病原体或其引起的损伤的手段。也称为模式识别受体(PRRs,pattern-recognition receptors),它们识别简单分子和分子结构的规则模式,称为病原体相关分子模式(PAMP, pathogen-associated molecular patterns (PAMPs)),是许多微生物的一部分,但不是宿主自身细胞的一部分。这些结构包括富含低聚糖、肽聚糖和细菌细胞壁的脂多糖,以及许多病原体常见的非甲基化CpG DNA(DNA中的非甲基胞嘧啶-鸟嘌呤二核苷酸)。所有这些微生物元素在进化过程中都被保存下来,使它们成为识别的绝佳目标,因为它们不会改变(图1.9)
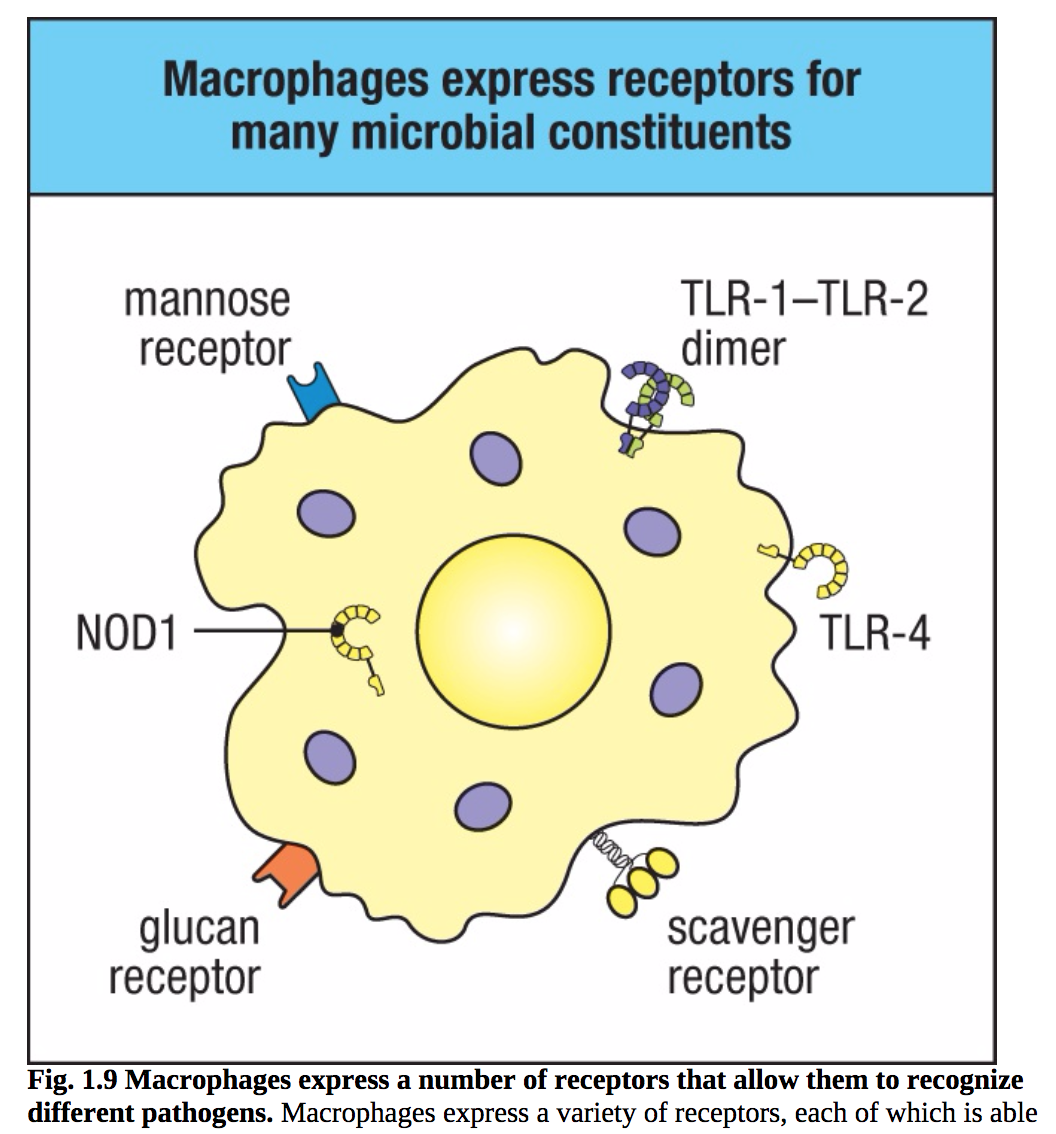
图1.9巨噬细胞表达多种受体,使其能够识别不同的病原体。巨噬细胞表达多种受体,每种受体都能识别微生物的特定成分。一些,如甘露糖、葡聚糖受体和清道夫受体(scavenger receptor),结合细菌、酵母和真菌的细胞壁碳水化合物。Toll样受体(TLRs)是巨噬细胞、树突状细胞和其他免疫细胞上的一个重要的模式识别受体家族。TLR识别不同的微生物成分;例如,TLR-1和TLR-2的异二聚体结合来自病原体(如革兰氏阳性菌)的某些脂肽,而TLR-4结合来自革兰氏阴性菌的脂多糖和来自革兰氏阳性菌的脂磷壁酸。其他模式识别受体是细胞内的,如核苷酸结合和寡聚结构域(NOD,nucleotide-binding and oligomerization domain)样受体。例如,NOD1与大多数革兰氏阴性菌细胞壁的一种成分二氨基戊酸结合
一些PRR是跨膜蛋白,如Toll样受体(TLR),其检测源自细胞外细菌或通过吞噬细胞作用进入囊泡途径的细菌的PAMP。Toll受体在免疫中的作用首先由Jules Hoffmann在果蝇中发现,后来由Charles Janeway和Bruce Beutler扩展到小鼠中的同源TLR。(Hoffmann和Beutler与Ralph Steinman共同获得了2011年诺贝尔奖,参见第1-4节,了解他们在激活先天性免疫方面的工作。)其他PRR是细胞质蛋白,如感觉细胞内细菌入侵的NOD样受体(NLR)。然而,其他细胞质受体基于宿主mRNA和病毒衍生RNA物种的结构和位置的差异以及宿主和微生物DNA之间的差异来检测病毒感染。传感器细胞表达的某些受体检测病原体引起的细胞损伤,而不是病原体本身。我们对先天认知的大部分知识是在过去二十年才出现的,现在仍然是一个活跃的发现领域。我们在第3章中进一步描述了这些先天的识别系统,并在第16章中讨论了佐剂如何用作疫苗的组成部分。
传感器细胞通过产生诸如趋化因子和细胞因子等介质来诱导炎症反应
参考资料
- Janeway’s Immunobiology 10th edition
